| РеЛеС.ру |
|
|||||||||||
| Действующие вещества | Торговые наименования | Фармакологический указатель | Нозологический указатель | Классификация АТХ | Производители |
|
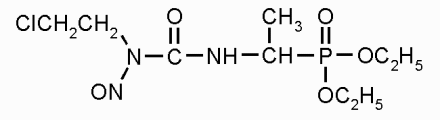
Наименование: Фотемустин* Наименование (лат.): Fotemustine* Брутто формула: "9"=="" ? "C " : "C9""19"=="" ? "H " : "H19"""=="" ? "Cl " : "Cl""3"=="" ? "N " : "N3""5"=="" ? "O " : "O5"""=="" ? "P " : "P" Химическое соединение: (±)-Диэтил-/1-/3-(2-хлорэтил)-3-нитрозоуреидо/этил/фосфонат CAS-код: 92118-27-9 Дата актуализации: 19/03/2002 Классификация по МКБ-10: Фармакологические группы: Фармакологическое действие:противоопухолевое (цитостатическое), алкилирующее, иммунодепрессивное Фармакология:Алкилирует и карбамоилирует нуклеофильные центры биомолекул в опухолевых клетках, действует циклонеспецифично. После однократного в/в введения связывается с белками крови на 25-30%, практически полностью метаболизируется. Легко проходит через гистогематические барьеры, включая ГЭБ, и хорошо проникает в клетки (пенетрацию облегчает наличие в химической структуре биоизомера аланина — амино-1-этилфосфоновая кислота). Характеристика:Производное нитрозомочевины. Растворим в 95% этиловом спирте и в метаноле, мало растворим в воде. Применение:Диссеминированная злокачественная меланома (особенно с метастазами в мозг), первичные злокачественные опухоли головного мозга. Противопоказания:Гиперчувствительность (в т.ч. к др. производным нитрозомочевины), гипоплазия костного мозга (число тромбоцитов менее 100·109/л, гранулоцитов — менее 2·109/л), беременность, кормление грудью, детский возраст (безопасность и эффективность применения у детей не определены). Ограничения к применению:Оценка соотношения риск-польза необходима при назначении в следующих случаях: угнетение функции костного мозга, предшествующая цитотоксическая или лучевая терапия. Применение при беременности и кормлении грудью:Противопоказано при беременности. На время лечения следует прекратить грудное вскармливание. Побочные действия:Тошнота и рвота через 2 ч после инъекции (47%), тромбоцитопения и лейкопения (40-46%) с максимальной выраженностью через 4-6 нед после первого введения, нарушение сознания, вкусовых ощущений, парестезии, боль в области живота, диарея, умеренное и обратимое повышение уровня мочевины (0,8%), трансаминаз, щелочной фосфатазы и билирубина в плазме (30%), гипертермия (3,3%), флебит в месте инъекции (3%), кожный зуд (0,7%). Взаимодействие:Усиливает респираторную токсичность дакарбазина. Другие миелотоксичные препараты и лучевая терапия могут потенцировать угнетение кроветворения. Меры предосторожности:Применение возможно только под наблюдением врача, имеющего опыт химиотерапии. До начала и во время лечения (с небольшими интервалами) необходимо определение уровня гемоглобина или гематокрита, билирубина, азота мочевины, креатинина, числа лейкоцитов (общее, дифференциальное), тромбоцитов. Очередной курс не рекомендуется проводить ранее 4-6 нед после окончания предшествующего курса. Не следует применять ранее, чем через 3 нед после введения дакарбазина (риск развития респираторного дистресс-синдрома). Во время лечения следует использовать адекватные меры контрацепции. В случае контакта препарата с кожей или слизистыми оболочками необходимо тщательное промывание водой (слизистые оболочки) или водой с мылом (кожа). Растворение, разведение и введение препарата проводится квалифицированным медицинским персоналом с соблюдением защитных мер (перчатки, маски, одежда и др.). Особые указания:Раствор для в/в введения готовят, добавляя к содержимому флакона прилагаемый растворитель (при этом получается 4 мл раствора, содержащего 200 мг фотемюстина). После расчета необходимой дозы раствор дополнительно разбавляют 5% раствором глюкозы. Приготовленный раствор следует использовать в течение 1 ч после приготовления. Литература:Булат Ю.В. Роль противоопухолевого препарата мюстофоран (фотемустин) в лечении больных с диссеминированной меланомой//Современная онкология.- 1999.- Т. 1.- N 1.- С. 27-29. Структурная формула: Торговые наименования: |